Jakarta
31 octobre – .
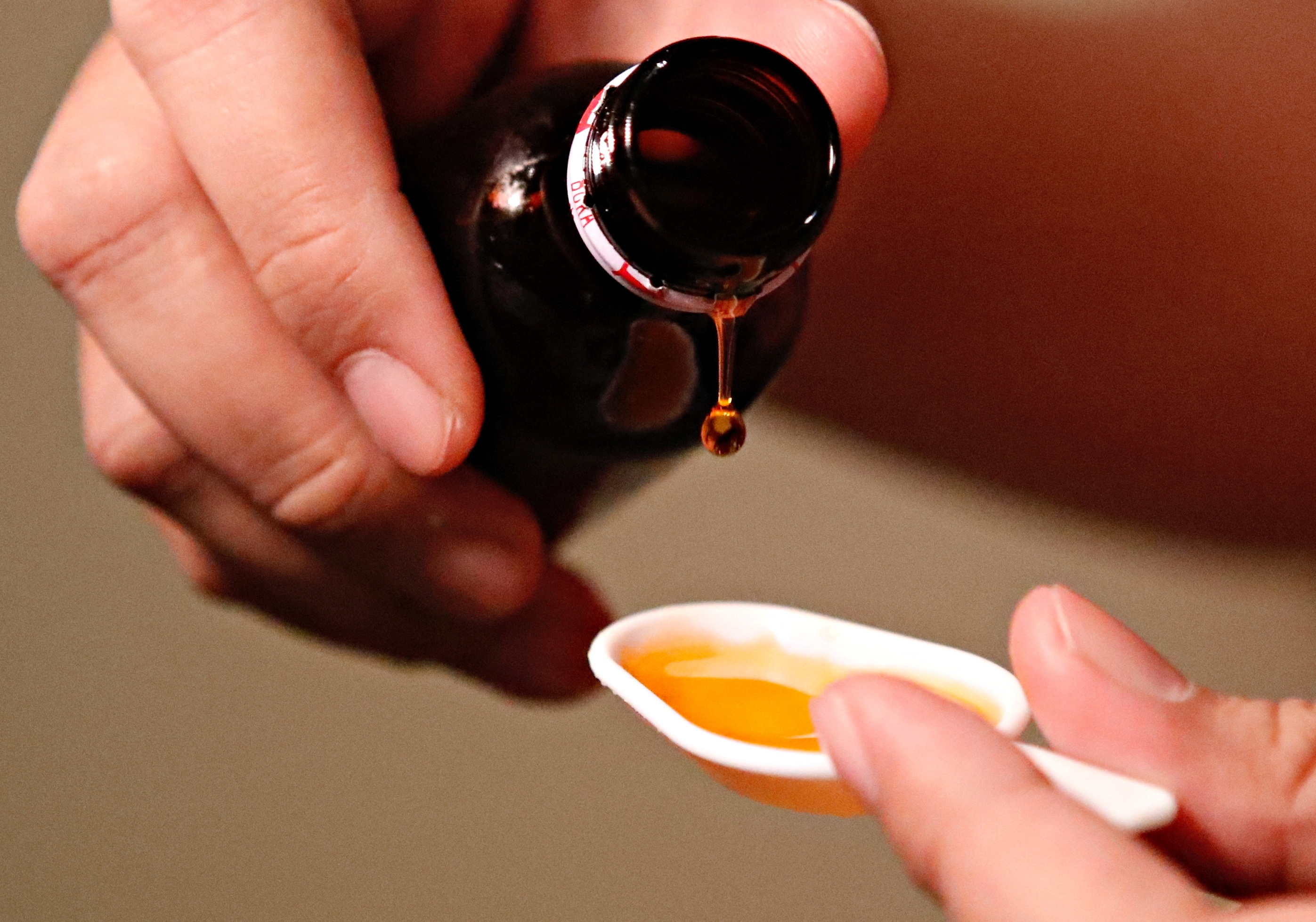
La décision intervient après que l’Indonésie a temporairement interdit la vente de certains médicaments à base de sirop et identifié la présence d’éthylène glycol et de diéthylène glycol dans certains produits comme un facteur possible de décès par AKI, dont la plupart étaient des enfants de moins de cinq ans.
Les deux sont utilisés dans les antigels et les liquides de frein et d’autres applications industrielles, mais sont également utilisés dans certains produits pharmaceutiques comme alternative moins chère à la glycérine, un solvant ou un épaississant dans de nombreux sirops contre la toux. Ils peuvent être toxiques et provoquer des lésions rénales aiguës.
Le chef de BPOM
Penny K. Lukito, a déclaré aux journalistes que deux sociétés, PT Yarindo Farmatama et PT Universal Pharmaceutical Industries, avaient vu leurs licences de fabrication de « liquide oral » révoquées, ajoutant que BPOM déposait des poursuites pénales contre elles.
Penny a déclaré que les deux sociétés utilisaient des matières premières de qualité inférieure pour fabriquer les médicaments, n’avaient pas signalé de changements dans les ingrédients et avaient utilisé des matériaux non conformes aux directives.
PT Yarindo Farmatama n’a pas immédiatement répondu à la demande de commentaires de Reuters
Un avocat de PT Universal Pharmaceutical Industries a refusé de commenter, citant une enquête en cours.
L’Indonésie a connu une augmentation des cas d’IRA chez les enfants depuis août
Ce qui, selon le ministre de la Santé du pays, était probablement dû à des changements dans les matières premières utilisées dans les sirops contre la toux et la fièvre.
Selon le ministère de la Santé
L’Indonésie importe principalement ses ingrédients pharmaceutiques de Chine et d’Inde.
Les autorités ont déclaré que les solvants utilisés dans les sirops des deux sociétés contenaient des impuretés.
L’un des solvants
Le propylène glycol, a été produit par Dow Chemical Thailand, a annoncé lundi BPOM. La société n’a pas immédiatement répondu à une demande de commentaire.
BPOM a déclaré qu’il enquêterait sur les distributeurs des deux fabricants de médicaments pour voir s’ils fournissaient des matériaux à d’autres fabricants de médicaments.
L’Indonésie a enquêté sur des cas d’IRA en consultation avec l’Organisation mondiale de la santé (OMS) à la suite d’un incident similaire survenu en Gambie plus tôt cette année, au cours duquel au moins 70 personnes sont décédées en relation avec un sirop fabriqué par l’Inde Maiden Pharmaceuticals.
💡 Source et référence
« Reuters.com », via : L’Indonésie révoque la licence de sirop anti-fièvre de l’entreprise tout en enquêtant sur 150 décès.
























